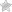Хронический миелолейкоз – заболевание крови опухолевого генеза, в основе которого лежит хромосомная перестройка с образованием химерного гена и усиленная пролиферация клеток-предшественников миелопоэза. В 95 % случаев у больных выявляется постоянная приобретенная хромосомная аномалия – так называемая филадельфийская хромосома (транслокация, то есть перемещение генетического материала дистальных (конечных) отделов длинных плеч 9 и 22 хромосомы).
Заболевание регистрируется во всем мире с примерно одинаковой частотой. Ежегодно выявляется 1 новый случай болезни на 100 тысяч населения. В структуре лейкозов на долю данной патологии приходится около 20 %. Хронический миелолейкоз встречается во всех возрастных группах, реже – у лиц моложе 20 лет. Пик заболеваемости приходится на 40-50 лет. Мужчины болеют несколько чаще, чем женщины.
Клинические проявления
У многих больных хронический миелолейкоз начинается исподволь. Нередко такой диагноз выставляется по анализу крови на фоне полного благополучия.
В клинической практике принято выделять 2 основные стадии болезни:
- Развернутая.
- Терминальная (с бластными кризами).
Развернутая стадия заболевания характеризуется моноклональностью (одинаковостью) клеток миелоидного ряда. При этом элементы нормального кроветворения практически вытеснены. В костном мозге выявляется большой процент клеток с филадельфийской хромосомой. Реже встречаются варианты заболевания с длительно сохраняющимся нормальным кроветворением.
На ранних этапах развития болезнь имеет либо бессимптомное, либо малосимптомное течение. Таких пациентов может беспокоить:
- немотивированная общая слабость;
- быстрая усталость и снижение работоспособности;
- отсутствие аппетита;
- повышенная потливость;
- тяжесть и болевые ощущения в левом подреберье (особенно после быстрой ходьбы или приема пищи).
У них увеличивается селезенка и печень, нарастают изменения в крови и костном мозге. Причем первые проявления болезни нередко связаны именно с большими размерами селезенки. Лимфатические узлы на начальных стадиях болезни обычно не поражаются.
При данной патологии страдает также фагоцитарное звено иммунитета. Это является причиной повышенной склонности к инфекционным заболеваниям и осложнениям.
Астенический синдром обусловлен повышенным клеточным распадом и особенностями продукции гранулоцитов, составляющих основную массу лейкоцитов.
При очень высоком уровне лейкоцитов (500×10⁹/л и более) в связи с их скоплением в сосудах и стазом крови возможно нарушение кровообращения в тканях (особенно в головном мозге) и желудочно-кишечные кровотечения.
Постепенно патологический процесс прогрессирует. В крови появляются анеуплоидные клетки с неправильным хромосомным набором, которые образуют новые субклоны опухолевых клеток, не способные к дифференцировке, то есть к образованию нормальных лейкоцитов, но быстро пролиферирующие (делящиеся) и подавляющие исходные дифференцирующиеся клетки. В этот период болезнь переходит в терминальную стадию. Самочувствие пациентов продолжает ухудшаться. Снижается эффективность ранее проводимого лечения. Клинически это проявляется:
- быстрым ростом размеров селезенки;
- лихорадкой с ознобами и проливными потами;
- сильными болями в костях;
- формированием очагов опухоли в лимфатических узлах;
- образованием лейкемидов на коже (представляют собой скопления опухолевых клеток; имеют вид пятен розоватого или коричневатого цвета);
- выраженной слабостью;
- истощением.
Течение болезни может быть различным. У одних больных оно относительно доброкачественное и лейкозный процесс развивается много лет. У других оно агрессивное с быстрым прогрессированием, приводящее в течение нескольких месяцев к гибели больного.
Изменения в крови
Первым признаком лейкоза могут быть изменения в анализе крови. У многих больных они появляются задолго до клинической манифестации болезни.
В развернутой стадии картина крови характеризуется:
- увеличением общего числа лейкоцитов (от 20 до 200×10⁹/л, а иногда и более);
- сдвигом в формуле крови до юных форм (промиелоцитов и метамиелоцитов);
- наличием единичных бластных клеток;
- увеличением процентного содержания базофилов и эозинофилов;
- ускорением СОЭ.
Количество тромбоцитов может оставаться нормальным или несколько снижаться. Однако в ряде случаев с самого начала болезни выявляется высокий тромбоцитоз (1500-2000×10⁹/л).
Красная кровь на ранних этапах патологического процесса существенно не меняется. Но у части больных уже в этот период появляется анемия.
Морфологически клетки крови практически не отличаются от таковых в норме. Однако некоторые особенности имеют гранулоциты:
- скудная зернистость;
- уменьшение содержания миелопероксидазы в миелоцитах, метамиелоцитах, нейтрофилах;
- снижение (иногда до нуля) щелочной фосфатазы в зрелых нейтрофилах.
По мере прогрессирования лейкоза и накопления опухолевых клеток увеличивается лейкоцитоз и ухудшается состояние больных. Вскоре болезнь переходит в терминальную стадию и показатели анализа крови еще больше усугубляются. При этом наблюдается:
- тромбоцитопения;
- анемия (рефрактерная к лечению);
- увеличение концентрации миелоцитов, промиелоцитов, бластов.
Характерным признаком болезни в терминальной стадии является бластный криз. Это состояние, при котором в крови и костном мозге растет содержание бластных клеток больше 20 %. Морфология клеток при бластном кризе отличается большим разнообразием. Они являются потомками колониеобразующих клеток, поэтому нередко имеют четкие признаки родоначальников того или иного клеточного ряда. Они могут быть:
- недифференцированные;
- миелобластные;
- лимфобластные;
- миеломонобластные;
- монобластные;
- эритробластные;
- мегакариобластные.
В связи с нарушением костномозговых барьеров в крови обнаруживаются осколки ядер мегакариоцитов и большое количество эритрокариоцитов.
В конечном итоге нормальное кроветворение полностью угнетается. Патологический процесс выходит за пределы костного мозга. Бластные клетки метастазируют в различные органы и ткани.
Постановка диагноза
Заподозрить наличие у больного хронического миелолейкоза врач может по характерным изменениям анализа крови и клиническим проявлениям. Особенно следует обратить внимание на немотивированный нейтрофильный лейкоцитоз с разной степенью омоложения лейкоцитарной формулы в сочетании с увеличением селезенки.
Для подтверждения диагноза должна проводиться трепанобиопсия костного мозга с исследованием его клеточного состава.
В развернутой стадии хронического миелолейкоза костный мозг богат клеточными элементами.
- В клеточном составе преобладают клетки гранулоцитарного ряда. Их соотношение с эритроцитами достигает 20:1 в пользу гранулоцитов.
- Процентное содержание бластов превышает 10 %.
- Может регистрироваться увеличенное количество мегакариоцитов с чертами дисплазии и избыточное выпадение ретикулиновых волокон.
- В терминальной стадии в костном мозге увеличивается число бластных клеток и соответственно снижается количество переходных форм и зрелых элементов.
В классических случаях трудностей с постановкой диагноза не возникает. Но они могут появляться при нерезко выраженных клинико-лабораторных изменениях. Тогда правильно поставить диагноз помогает цитогенетическое и молекулярно-генетическое исследование. Они позволяют выявить филадельфийскую хромосому и другие хромосомные поломки.
Дифференциальная диагностика проводится:
- с лейкемоидными реакциями (в ответ на инфекцию, опухоль);
- идиопатическим миелофиброзом;
- эссенциальной тромбоцитопенией;
- хроническим миеломоноцитарным лейкозом и т. д.
Общие принципы лечения
Лечение хронического миелолейкоза неоднозначно и зависит от стадии болезни, тяжести ее течения. Оно направлено:
- на уменьшение опухолевой массы;
- нормализацию состава крови;
- повышение качества жизни больных;
- увеличение ее продолжительности.
Основными методами лечения являются:
- химиотерапия;
- трансплантация костного мозга.
В настоящее время для химиотерапии используются:
- гидроксимочевина (применялась для лечения хронического миелолейкоза больше половины столетия; с ее помощью удавалось снизить количество опухолевой массы и добиться нестойкой ремиссии);
- препараты α-интерферона (считаются более эффективными, но имеют много побочных явлений);
- ингибиторы тирозинкиназы (хорошо переносятся больными, вызывают мало побочных эффектов; угнетают пролиферацию опухолевых клеток, практически не влияя на здоровые аналоги; однако эффективны не у всех больных, что связано с развитием резистентности).
Алогенная трансплантация костного мозга является единственным методом, позволяющим излечить больного. Но риск осложнений после нее остается высоким и составляет около 20-40 %.
В настоящее время продолжается поиск новых программ лечения данной патологии, которые смогли бы полностью подавить опухолевый клон с целью увеличения выживаемости.
К какому врачу обратиться
Первые проявления болезни, связанные с увеличением в крови пациента лейкоцитов, может отметить любой врач по результату общего анализа крови с лейкоцитарной формулой. В дальнейшем лечением больных занимается онкогематолог.
Прогноз
Прогноз при хроническом миелолейкозе малоблагоприятный. Современные методы лечения позволяют продлить жизнь таким больным, однако летальность остается высокой. Тяжелее протекает болезнь у лиц пожилого возраста с выраженной спленомегалией, тромбоцитопенией, высоким содержанием бластов в крови и костном мозге.