Фенилкетонурию еще называют фенилпировиноградной олигофренией в связи с тяжелым поражением центральной нервной системы фенилпировиноградной кислотой и другими производными фенилаланина. Это наследственное заболевание, в основе которого лежит ферментативная недостаточность и нарушение метаболизма аминокислот, в частности – фенилаланина. Больные дети часто рождаются от здоровых родителей, которые являются переносчиками мутантного гена. Девочки болеют несколько чаще, чем мальчики.
Частота встречаемости данной патологии различна в разных странах мира. Так, в России 1 случай болезни приходится на 8-10 тысяч новорожденных, тогда как в Японии – 1:100000. Практически не встречается она у представителей негроидной расы и евреев-ашкенази.
Почему возникает

В настоящее время медицинской науке известно несколько видов фенилкетонурии, которые имеют не только разные причины, но и свои особенности течения. Среди них можно выделить 3 основных:
- Классическая фенилкетонурия. Это заболевание, связанное с мутацией гена, расположенного на длинном плече 12 хромосомы, который кодирует активность фермента фенилаланин-4-гидроксилазы. Он обеспечивает превращение фенилаланина в тирозин. Вследствие дефицита этого фермента (выраженность его может быть различной) в тканях накапливаются фенилаланин и его производные (фенилпировиноградная, фенилмолочная, фенилуксусная кислота и др.).
- Фенилкетонурия 2-го типа. При данной патологии также нарушается процесс метаболизма фенилаланина, но механизм его несколько иной. Генный дефект располагается в 4 хромосоме. Он приводит к дефициту фермента дигидроптеридинредуктазы, участвующего в восстановлении активной формы тетрагидробиоптерина, который необходим в организме для гидроксилирования аминокислотных остатков.
- Фенилкетонурия 3-го типа. Этот вариант болезни связан с недостаточностью другого фермента, который обеспечивает синтез тетрагидробиоптерина. Вследствие дефицита последнего формируются метаболические блоки на пути преобразования фенилаланина в тирозин.
Продукты метаболизма этой аминокислоты оказывают токсическое воздействие на головной мозг, что приводит к нарушению нейропсихического развития у ребенка и необратимым изменениям в нервной системе. Усугубляет состояние больных дефицит катехоламинов и меланина, возникающий в организме из-за недостаточного образования тирозина.
Существует определенная зависимость между особенностями клинической картины заболевания и степенью активности пораженного фермента.
- При полном отсутствии ферментов у человека обнаруживаются все характерные черты заболевания.
- При частичном снижении их активности выявляется различная степень задержки развития и церебральные нарушения.
Симптомы классической фенилкетонурии
Ферментативная недостаточность проявляет себя в первые 6 месяцев жизни. Причем при рождении сложно заметить какие-либо отклонения. Новорожденный выглядит вполне здоровым. Только иногда могут выявляться аномалии развития скелета и внутренних органов. У большинства таких детей имеются признаки гипопигментации:
- бледная кожа;
- светлые волосы;
- голубые глаза.
Первые симптомы обнаруживаются у ребенка на 2-6-м месяце жизни. К ним относят:
- вялость;
- слабый интерес к окружающему миру (или его отсутствие);
- беспокойство;
- высыпания на коже (по типу дерматитов, экземы);
- повышенная чувствительность кожи к травматизации;
- судороги;
- «мышиный запах» (выделение с мочой фенилацетата);
- срыгивание и рвота.
Позже становится заметным отставание в развитии. Особенно страдает нейропсихическая сфера и формирование интеллекта. В психологическом статусе больных отмечают:
- несформированность игровой и предметной деятельности;
- отсутствие дифференцировки эмоциональных реакций;
- речевые расстройства.
Дети не стремятся к общению с родителями, эмоции их обеднены. Большая часть таких лиц имеют идиотию или олигофрению. Но в литературе описаны отдельные случаи заболевания, когда у ребенка был выявлен нормальный интеллект.
Физическое развитие у больных нарушено в меньшей мере, но признаки его изменения также имеют место при этом заболевании:
- низкий рост;
- запоздалое прорезывание зубов;
- малые размеры черепа;
- характерная поза у ребенка (стоит, опустив голову и широко расставив ноги, согнутые в коленях и тазобедренных суставах; сидит, поджимая ноги);
- изменение походки (покачивание и передвижение мелкими шажками) и др.
Такие дети поздно начинают сидеть и ходить. У них наблюдаются различные неврологические расстройства:
- тремор конечностей (дрожание);
- гиперкинезы (внезапно возникающие непроизвольные движения);
- эпилептические припадки;
- атаксия.
Нарушения работы внутренних органов для фенилкетонурии не типичны, если нет врожденных пороков.
Атипичные формы болезни
К ним относят фенилкетонурию 2-го, 3-го типа и другие редко встречающиеся варианты патологического процесса. Для каждого из них характерны свои особенности течения, но среди них можно выделить и общие черты:
- ранняя манифестация (проявляет себя с первых недель жизни);
- тяжелая умственная недостаточность;
- наличие признаков повышенной возбудимости и гиперрефлексии;
- спастический тетрапарез (не функционируют все 4 конечности) и др.
Болезнь быстро прогрессирует. Ее исход может быть неблагоприятным (смерть в возрасте 2-3 лет).
Диагностика
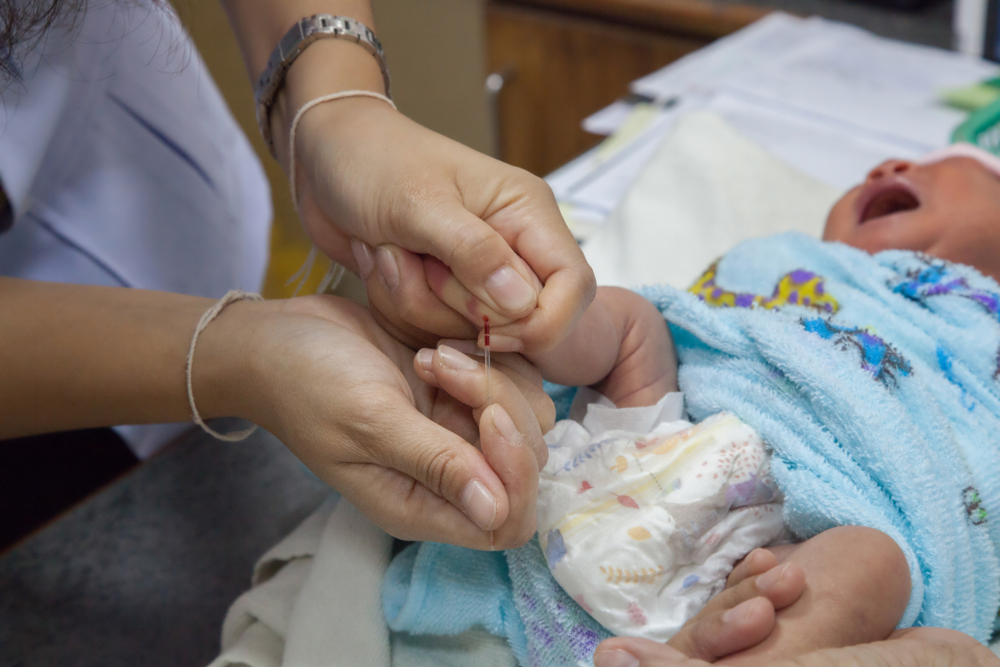
Чем раньше ребенку поставлен диагноз «фенилкетонурия», тем лучше прогноз и больше вероятность нормального развития интеллекта.
В связи с высокой распространенностью данной патологии, тяжестью течения и реальной возможностью профилактического лечения ВОЗ включила ее в список наследственных заболеваний, для выявления которых проводится массовый скрининг новорожденных. Все дети на 4-5-й день жизни должны обследоваться на фенилкетонурию. Для этого у ребенка производят забор крови, пропитывают ее каплей специальный бланк и отправляют на исследование в лабораторию медико-генетического центра. По результатам этого анализа (уровень фенилаланина) оценивают вероятность развития болезни у ребенка.
- При обнаружении стойкой гиперфенилаланинемии проводится дифференцирование классической формы болезни от атипичных.
- При незначительном увеличении концентрации этой аминокислоты в крови проводятся повторные анализы.
В более старшем возрасте предположить наличие заболевания у ребенка врач может на основании клинических данных. Особенно высокий риск его развития имеют дети, в семьях которых уже регистрировались случаи болезни. Подтвердить диагноз позволяют лабораторные исследования:
- определение уровня фенилаланина в крови (более 900 мкмоль/л);
- выявление его производных в моче (проба Феллинга);
- обнаружение дефектных генов с помощью молекулярно-генетических методов (полимеразно-цепная реакция).
Лечение
Основу лечения больных фенилкетонурией составляет лечебное питание. Причем чем раньше оно начато, тем лучше его результаты.
Специфическая диета назначается незамедлительно после постановки диагноза (желательно с первых дней жизни по результатам скрининга). Рацион больного ребенка составляют по принципу резкого ограничения фенилаланина, содержащегося в пище. Для этого из него исключают продукты, богатые белком:
- блюда из мяса или рыбы;
- сосиски и колбасы;
- творог и твердый сыр;
- яйца;
- хлеб и выпечка;
- крупы и бобовые;
- орехи;
- шоколад.
Фенилаланин относится к числу незаменимых аминокислот, поэтому для обеспечения нормального роста и развития ребенка это соединение должно присутствовать в рационе, но в минимальных количествах. Питание таким детям назначают соответственно возрасту и массе тела.
К числу разрешенных продуктов относят:
- овощи;
- молоко;
- сливочное и растительное масло;
- фрукты;
- сахар;
- безбелковые крупы, макароны, хлеб;
- амилофены (малобелковые крахмалсодержащие продукты);
- мед;
- джем, варенье.
Количество белка, полученного естественным путем (с пищей), в диете рассчитывают с учетом содержания в продуктах фенилаланина и допустимых его суточных количеств. На его долю приходится не более 20-22 % от возрастной физиологической нормы. Недостающее количество протеинов восполняют за счет специально разработанных лечебных продуктов, которые частично или полностью лишены токсичного для таких лиц химического соединения:
- гидролизаты белка (Афенилак, Лофеналак, Нофелан);
- смеси аминокислот (Тетрафен, Фенил-Фри).
Также в состав этих смесей входят:
- витамины;
- микроэлементы;
- полиненасыщенные жирные кислоты.
Следует отметить, что некоторые из этих продуктов имеют неудовлетворительные органолептические свойства. Детям не нравится их вкус и запах. Это может вызывать снижение аппетита, отказ от еды, тошноту и даже рвоту. В таких случаях необходимо уменьшить дозу смеси или заменить ее на другую. Более современные лечебные продукты (Афенилак, Тетрафен) хорошо переносятся детьми. Для предотвращения диспепсических явлений их постепенно вводят в рацион больного, начиная с малых доз. Необходимое суточное количество гидролизата разделяют на несколько приемов и назначают после еды с грудным молоком, соком, компотом.
Важная особенность диетического лечения – строгий контроль содержания фенилаланина в сыворотке крови. На начальных этапах лечения его проверяют 1 раз в неделю, при достижении целевых значений – 1 раз в месяц, а у детей старше года – 1 раз в 2-3 месяца.
Отмену диетотерапии начинают не ранее 10-летнего возраста, когда нервная система уже не так чувствительна к фенилаланину. Расширение рациона проводят в течение нескольких недель. При этом контролируют изменение лабораторных показателей и состояние ребенка. Для лиц женского пола вопрос о продолжительности лечебного питания имеет особое значение, так как в будущем, при желании иметь детей, им рекомендуют соблюдать элементную диету до наступления беременности и в течение всего периода вынашивания ребенка.
Из медикаментов таким пациентам назначают:
- витаминные комплексы;
- ноотропные средства (Церебролизин, Энцефабол);
- лекарственные средства, улучшающие микроциркуляцию (Трентал);
- препараты, нормализующие тканевой обмен (цитохром С, АТФ);
- аминокислоты с разветвленной цепью – лейцин, изолейцин, тирозин (конкурентное ингибирование транспортных систем).
В настоящее время поиск новых методов лечения фенилкетонурии продолжается. Предприняты попытки лечения больных растительным ферментом, способным превращать токсичную аминокислоту в безвредные метаболиты. У некоторых больных эффективно применяется кофактор пораженного фермента (тетрагидробиоптерин).
Атипичные формы болезни в большинстве случаев малочувствительны к диетотерапии. Таким лицам обычно назначается тетрагидробиоптерин.
Заключение

Фенилкетонурия – тяжелое заболевание, которое без квалифицированной помощи имеет крайне неблагоприятный прогноз. Лечение таких детей сопряжено с определенными сложностями. Оно требует своевременного начала и постоянного медицинского контроля. Разные пациенты по-разному реагируют на диетотерапию, что в первую очередь зависит от формы болезни. У большей части из них удается добиться удовлетворительных результатов лечения и сохранения интеллекта (обычно при классическом течении болезни). При позднем начале терапии (если ребенку больше 1 года) она не эффективна.
О фенилкетонурии в программе «Жить здорово!» с Еленой Малышевой:
